糖尿病足溃疡是糖尿病的严重并发症之一,会显著增加糖尿病患者的截肢率和死亡率。糖尿病溃疡低效愈合的重要因素被广泛认为是由于伤口中的高活性氧(ROS)水平造成的氧化应激和炎症反应,从而导致抗氧化酶功能减退及功能细胞的恶化,如干细胞的增殖和分化不良。因此,开发具有ROS清除能力的仿酶材料来减轻氧化应激和缓解炎症环境可以为促进难治性伤口愈合提供机会。近年来,人们设计了多样化的过渡金属化合物和金属纳米颗粒类生物催化剂来模拟天然抗氧化酶功能,但ROS催化过程涉及多电子反应,复杂的中间键形成,以及最终解吸氧物质高能量消耗,与天然抗氧化酶相比,目前已建立的金属化合物基类抗氧化酶生物催化剂很难模拟这一复杂的氧化还原过程。因此,寻找一种合适的策略来克服不平衡的多电子反应,实现具有超快动力学的可逆催化循环,开发出超快和广谱抗氧化酶样催化结构仍然是一个巨大挑战。
基于此57365线路检测中心通道内分泌科/糖尿病中心陈秋教授团队联合四川大学研究团队构建了一种具有非晶态Ru@CoSe纳米层的硒化钴基生物催化剂,具有超快和广谱催化ROS清除的活性,可有效地挽救在氧化应激环境下人骨髓间充质干细胞(hMSCs)的生存状态及其血管生成潜能,同时可以显著促进糖尿病创面愈合。
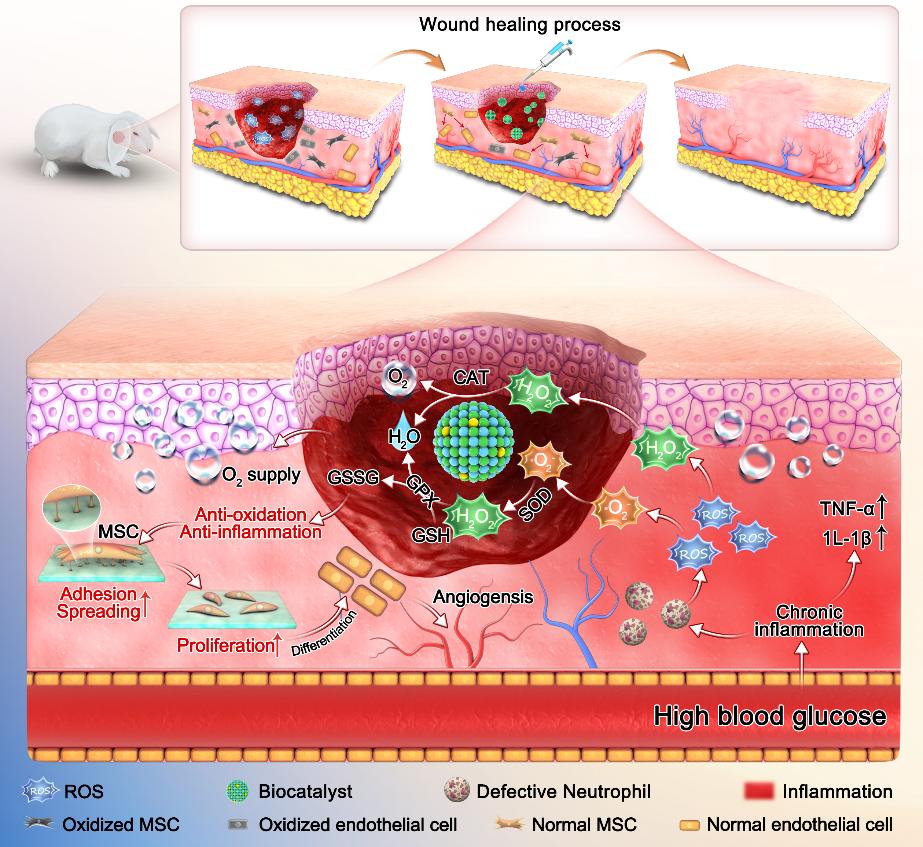
Ru@CoSe仿酶纳米材料在清除ROS,保护干细胞,促进血管生成和糖尿病伤口愈合的工作机制示意图
该研究为催化ROS清除和促进慢性炎症伤口愈合提供了一种有效的纳米药物,并通过引入无定形催化结构为设计生物催化金属化合物提供了新思路。相关成果以“Amorphizing Metal Selenides-Based ROS Biocatalysts at Surface Nanolayer toward Ultrafast Inflammatory Diabetic Wound Healing”为题发表在国际知名权威期刊ACS Nano(中科院/JCR 1区Top期刊, IF=18.027)上。成都中医药大学临床医学院高阳博士为本文的共同第一作者,57365线路检测中心通道内分泌科/糖尿病中心陈秋教授为共同通讯作者。

文章原文链接:https://pubs.acs.org/doi/abs/10.1021/acsnano.2c11448


 订阅号
订阅号
 公众号
公众号